
An inherently kidney-targeting near-infrared fluorophore based probe for early detection of acute kidney injury. Biosensors and Bioelectronics
用于活性氧检测的近红外荧光探针在急性肾损伤中的应用
Fangqin Wang, Xuefeng Jiang, Huaijiang Xiang, Ning Wang, Yunjing Zhang, Xi Yao, Ping Wang, Hao Pan, Lifang Yu, Yunfeng Cheng, Yongzhou Hu, Xin Li, Weiqiang Lin. DOI: 10.1016/j.bios.2020.112756
主讲人:俞容 2024.4.21
研究进展:
急性肾损伤(AKI)是常见且重要的临床疾病,其发生由多种致病因素引起,包括败血症、缺血再灌注和肾毒性药物等。对AKI的早期诊断至关重要,因为只有在早期阶段才能治疗和逆转该病情。延迟或未能及时识别AKI可能导致疾病进展、治疗负担加重、恢复受损以及高死亡率。因此,早期诊断和干预是治疗AKI并改善预后的关键。目前,监测血清肌酐和血尿素氮是诊断AKI的标准工具,但它们更反映肾功能而非肾损伤程度,因此对早期检测的效用有限。鉴于此,迫切需要更敏感的生物标志物和诊断方法。
许多研究表明,过氧亚硝酸盐(ONOO-)在AKI的发病机制中起着重要作用,可能是导致AKI早期损伤的主要原因。一氧化氮和超氧阴离子在AKI的初始阶段失衡,但直到它们相遇并转化为ONOO-时才具有破坏性。ONOO-具有高度氧化性和破坏性,可通过与脂质、DNA和蛋白质直接或间接作用,导致细胞损伤、炎症和凋亡,进而诱发AKI。因此,检测肾脏中的ONOO-与AKI的早期诊断密切相关。然而,由于ONOO-在生理环境中的寿命极短,传统的生物学测定法难以分离组织并测量其含量。尽管细胞内的3-硝基酪氨酸免疫组织学定量已广泛用于间接分析过氧亚硝酸盐,但这种方法侵入性较高、技术要求严格,限制了其临床应用。近年来,随着对ONOO-在各种疾病中病理作用认识的深入,对其原位成像的研究日益增多。虽然在肾脏中实现非侵入性荧光成像具有挑战性,但随着对成像剂的改进和探针与过氧亚硝酸盐结合的研究不断深入,这一领域的发展前景仍然广阔。
研究内容:
在这项研究中,作者团队设计了一种名为KNP-1的探针,该探针是专门用于早期诊断AKI的高对比度荧光成像。KNP-1的设计基于其固有的肾脏靶向性和对ONOO−的敏感荧光反应。本文发现,在患有AKI的活小鼠中,甚至在AKI发作时,使用KNP-1进行成像可以得到良好的肾脏对比成像结果。此外,随着AKI的进展,通过时间分辨率成像显示了肾脏中ONOO−水平的逐渐增加,突显了ONOO−作为前体生物标志物和KNP-1作为AKI早期检测敏感工具的重要性。这项研究为开发新型AKI诊断工具提供了有力的支持,具有重要的临床应用前景。
要点:
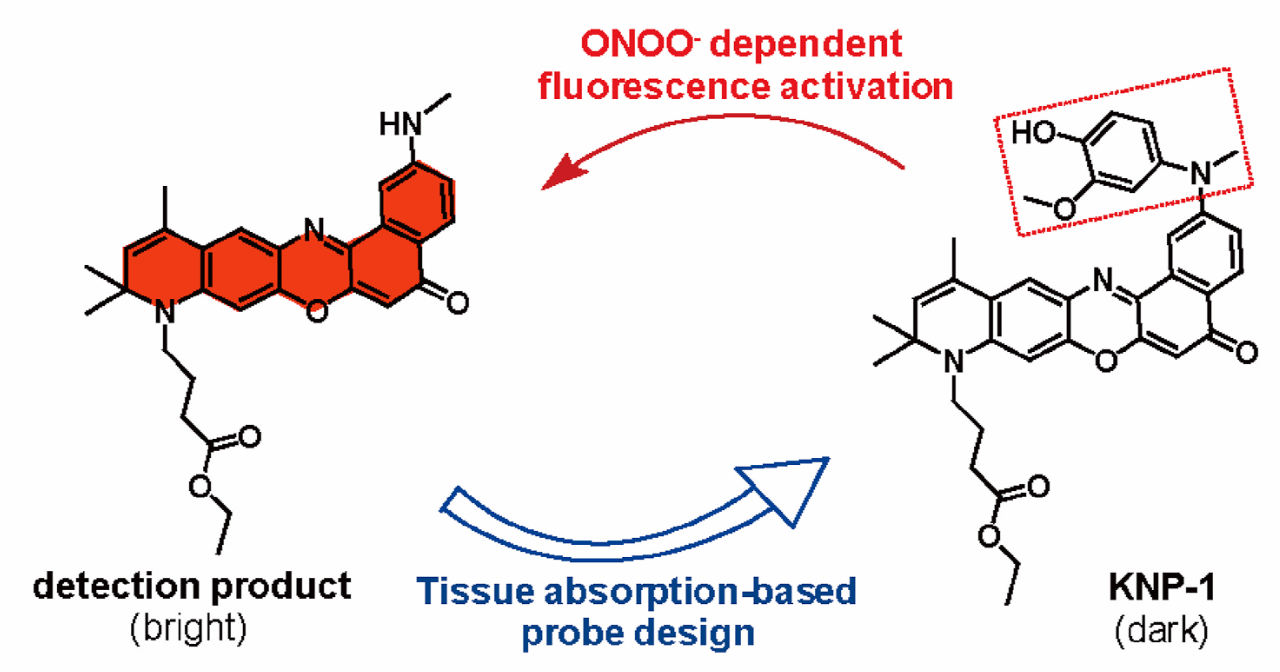
1. 作者团队以尼罗红衍生物为荧光基团,氢化喹啉基团为识别基团,开发了一种肾脏靶向探针KNP-1,可以特异性识别ONOO−。
2. 探针KNP-1对AKI时上调的ONOO−敏感响应,同时具有良好的肾脏靶向性,并应用于AKI小鼠活体成像中能观察到良好的肾脏成像效果。
3. 随着AKI的进展,实时成像显示肾脏中ONOO−水平逐渐上升,其荧光变化比传统的血清学检查如肌酐(sCr)和尿素氮(BUN)至少提前24小时监测到AKI的发生。
总结与展望:
作者团队通过开发基于肾吸收荧光团的探针KNP-1,实现了对AKI的高对比度肾脏成像。KNP-1静脉注射后快速分布到小鼠肾脏中,并对在AKI早期就出现上调的活性氧ONOO−产生荧光响应。这种高对比度成像的实现得益于两个关键设计原则:一是KNP-1基于肾脏靶向能力的设计,使其能够快速分布在肾脏中,从而获得良好的对比度;二是KNP-1荧光的特性,只能由ONOO−触发的识别基团氧化裂解来产生,这使得其对早期AKI发病时ONOO−上调的敏感性得以体现。活体成像验证了KNP-1在AKI可视化中的适用性。值得一提的是,KNP-1荧光信号比传统的sCr和BUN水平至少提前24小时指示AKI的发生。这项研究强调了基于吸收的探针设计策略用于探索高组织对比度成像模式的可行性,并突显了KNP-1作为AKI早期检测的有用工具的潜力。

